肌肉的一张一弛是我们生命必不可少的,几乎每时每刻身体里都有肌肉在收缩。运动的时候需要肌肉收缩,这个好理解,其实睡眠时,也需要肌肉收缩,要不然我们没有办法维持呼吸。控制肌肉收缩的一个重要结构是神经肌肉接头(neuromuscular junction, NMJ),这是运动神经元与骨骼肌纤维之间的一个接点,负责将运动神经的信号传递给肌肉,产生肌肉收缩。NMJ是一个化学突触,神经末梢释放乙酰胆碱(ACh),其作用于肌纤维上的乙酰胆碱受体(AChR),使得肌肉纤维兴奋。NMJ高效的信号传递需要神经末梢和肌肉纤维的高度分化,比如在神经末梢接触到肌肉的地方有高密度的AChR聚集。NMJ发育异常或功能障碍可导致肌无力、呼吸衰竭等疾病。
NMJ的形成需要运动神经元释放的聚集素(agrin),其结合肌纤维膜上LRP4,形成四聚体复合物,进而激活肌肉特异性受体酪氨酸激酶(MuSK),诱导AChR聚集、促进NMJ形成。MuSK下游有两个蛋白对AChR聚集非常重要,一个是接头蛋白Dok7,它与MuSK的结合可以增强MuSK激酶活性,它还与一些下游分子如CRK或CRKL结合,促进AChR聚集。另外一个蛋白质是rapsyn,它是一个经典的支架蛋白,有三个功能域:TPR(Tetratricopeptide Repeats)结构域 ,可以结合许多蛋白质,包括MACF1,β-Catenin, α-actinin,Plectin,HSP90β 和Calpain;coiled-coil(CC)结构域结合AChR的β亚基(β-subunit);RING结构域和β-dystroglycan结合。
有意思的是rapsyn的RING结构域具有E3泛素连接酶的关键特征,如"C3H2C3"的锌指模体(其中C为半胱氨酸,H为组氨酸)。梅林团队在2016年发现rapsyn具有E3连接酶活性(Li et al., Neuron 2016)。重组rapsyn RING结构域在体外能与E1/E2连接酶共同催化自身泛素化。锌指模体关键位点C366的突变,不仅消除了rapsyn在异源细胞中诱导AChR聚集的能力,也削弱了其对rapsyn缺失小鼠NMJ缺陷的挽救功能。C366A敲入小鼠完全丧失NMJ形成能力。这些结果表明,rapsyn的E3酶活性对形成NMJ十分重要。
然而,rapsyn究竟如何通过E3连接酶活性调控NMJ形成的分子机制仍不清楚。E3连接酶可介导多种修饰,包括泛素化(ubiquitination)、类泛素化(neddylation)和SUMO化(sumoylation)。梅林团队前期研究提示rapsyn可能是一个类泛素化 E3连接酶,通过催化底物蛋白与Nedd8的结合来稳定AChR,介导NMJ组装。但是这个假说没有直接的遗传学证据。
近期,首都医学科学创新中心梅林团队在神经科学会的期刊Journal of Neuroscience上发表文章,试图回答这个问题。文章题目为“Neddylation E1 obligatory subunit Nae1 is critical to neuromuscular junction development and maintenance”。研究发现Neddylation E1必要亚基Nae1对神经肌肉接头的发育与维持至关重要。

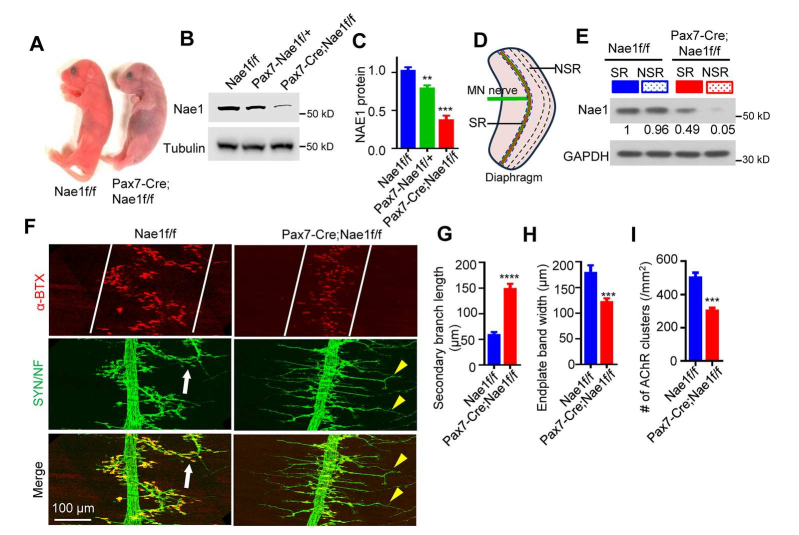
类泛素化与泛素化类似,需要E1激活酶、E2结合酶和E3连接酶(如rapsyn)依次催化完成。E2有多个,如Ubc12、Ubc2F等,都可以与rapsyn结合,靶向E2酶验证类泛素化假说具有技术难度。因此他们选择靶向类泛素化 E1酶,该酶由两个必需亚基Nae1(APP-BP1)和Uba3组成。利用配对盒转录因子7(Pax7)特异驱动的重组酶小鼠,他们敲除小鼠肌肉中Nae1,发现突变小鼠出生后很快会因窒息死亡,NMJ的表型与rapsyn缺失或E3连接酶活性缺失突变体(C366A)相似,包括AChR聚集体数量和面积缩小, AChR密度下降等。此外,突触前神经末梢分支增多,部分末梢甚至延伸至肌肉纤维外周区域,提示突触前-后信号协调异常。
突变小鼠在胚胎发育早期(E14),未受神经支配的AChR聚集体数量、大小和密度均显著减少。到了E15.5阶段,神经诱导的AChR聚集体形成也受到抑制,且突触前神经分支异常增多。值得注意的是,尽管E15.5时大部分AChR聚集体仍能被神经末梢覆盖,但到了E17.5和出生后(P0),突变小鼠中出现了大量无AChR聚集体的“裸露”神经末梢,表明类泛素化缺失可能导致突触后结构的维持障碍。


